A reação de decomposição da amônia (NH3) pode produzir hidrazina (N2H4) e gás hidrogênio (H2), conforme a equação química que se segue. Essa reação ocorreu a...
2022
CESPE / CEBRASPE
A reação de decomposição da amônia (NH3) pode produzir hidrazina (N2H4) e gás hidrogênio (H2), conforme a equação química que se segue.
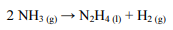
Essa reação ocorreu a partir de 0,07 m3 de uma mistura gasosa que possui 70% em massa de amônia e cuja densidade é 0,9 g/L. A eficiência do processo foi de 65% e foram observadas as seguintes reações químicas e respectivas variações de entalpia (∆Hn, em que n = 1 ou 2):

Nessa situação hipotética, considerando-se que 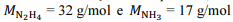 sejam as massas molares da hidrazina e da amônia, respectivamente, a variação de entalpia envolvida na quebra da amônia, caso o rendimento da reação tivesse sido de 100%, seria
sejam as massas molares da hidrazina e da amônia, respectivamente, a variação de entalpia envolvida na quebra da amônia, caso o rendimento da reação tivesse sido de 100%, seria