O ferro metálico, amplamente utilizado na indústria, pode ser obtido a partir da redução do óxido ferroso (FeO) pelo monóxido de carbono (CO), de acordo com ...
2022
CESPE / CEBRASPE
O ferro metálico, amplamente utilizado na indústria, pode ser obtido a partir da redução do óxido ferroso (FeO) pelo monóxido de carbono (CO), de acordo com a equação abaixo, cuja variação de entalpia é desconhecida.
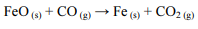
Caso essa reação seja realizada em etapas, as reações de cada etapa serão as seguintes, em que ∆Hn (n = 1, 2 ou 3) representa a variação de entalpia da n-ésima etapa:
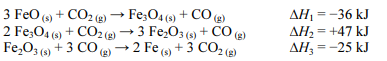
A partir da Lei de Hess, é possível calcular a variação de entalpia envolvida na primeira reação. Nessa situação, considerando-se que MFe = 56 g/mol seja a massa molar do ferro, é correto concluir que a variação de entalpia envolvida na formação de 140 g de ferro metálico por meio da redução do óxido ferroso pelo monóxido de carbono é