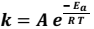A dependência da cinética química em relação à temperatura tem sido estudada extensivamente. Para diversas reações, uma relação empírica, chamada de equação ...
2021
INSTITUTO AOCP
A dependência da cinética química em relação à temperatura tem sido estudada extensivamente. Para diversas reações, uma relação empírica, chamada de equação de Arrhenius, pode ser usada para descrever a dependência da constante de velocidade (k) em relação à temperatura:
Nessa equação, Ea é a energia de ativação, R é a constante dos gases, T é a temperatura absoluta e A, o fator de frequência (considerado aproximadamente constante). Com base nessa relação empírica descrita, assinale a alternativa correta.